中科院合肥研究院強磁場(chǎng)中心張欣課題組發(fā)現ULK1/ATG13調控細胞分裂期自噬及腫瘤生長(cháng)的重要機制,相關(guān)論文以“ULK1-ATG13 and their mitotic phospho-regulation by CDK1 connect autophagy to cell cycle”為題發(fā)表在生物學(xué)權威期刊PLOS Biology上。
自噬和細胞周期調控都是極其動(dòng)態(tài)的基本生物學(xué)過(guò)程,而自噬在細胞周期調控中的功能與分子機制還不清楚。自噬是真核生物中發(fā)現的保守降解機制,主要有自噬相關(guān)蛋白(ATG)執行自噬過(guò)程,ULK1/ATG13是最上游的自噬起始復合物。細胞周期由間期和分裂期組成;一般而言,非同步化細胞中細胞間期和分裂期時(shí)間比例是95%、5%。在非同步化細胞中,ULK1/ATG13主要受到mTORC1和AMPK磷酸化以調控自噬起始。然而,在有絲分裂期及細胞周期各階段,ULK1/ATG13的磷酸化調控及功能尚不清楚。
張欣課題組研究發(fā)現:自噬起始蛋白ULK1/ATG13受到了細胞周期最重要激酶CDK1的磷酸化調控,以促進(jìn)有絲分裂期自噬及細胞周期進(jìn)程;另一方面發(fā)現ULK1/ATG13復合物雙敲除不僅能夠顯著(zhù)抑制腫瘤細胞生長(cháng),而且荷瘤小鼠模型顯示對腫瘤抑制的效果達到了95%。
因在細胞自噬機制方面的發(fā)現而獲得2016年諾貝爾生理或醫學(xué)獎的大隅良典(Yoshinori Ohsumi)對本項工作進(jìn)行了專(zhuān)評,發(fā)表在同期的PLOS Biology上。專(zhuān)評指出:在本刊中,李等人發(fā)現了CDK1在有絲分裂期磷酸化ULK1復合物。這種磷酸化誘導自噬,并且出人意料的可以驅動(dòng)細胞周期進(jìn)程……這項工作揭示了自噬在細胞周期進(jìn)程中的作用,并加強了我們對細胞生長(cháng)和增殖特定時(shí)相中自噬調控的理解(專(zhuān)評題為Mitotic phosphorylation of the ULK complex regulates cell cycle progression,鏈接:(https://journals.plos.org/plosbiology/article?id=10.1371/journal.pbio.3000718)
助理研究員李志元為該論文第一作者兼共通訊作者,博士后田小飛、助理研究員紀新苗、研究生王君君、陳含笑及王冬梅參與了該工作,張欣研究員為通訊作者。該項工作得到了國家重點(diǎn)研發(fā)項目、合肥物質(zhì)科學(xué)技術(shù)中心重要/創(chuàng )新項目培育基金、合肥研究院十三五重點(diǎn)項目及院長(cháng)基金、國家自然科學(xué)基金和安徽省基金的支持。
原文鏈接:https://doi.org/10.1371/journal.pbio.3000288。
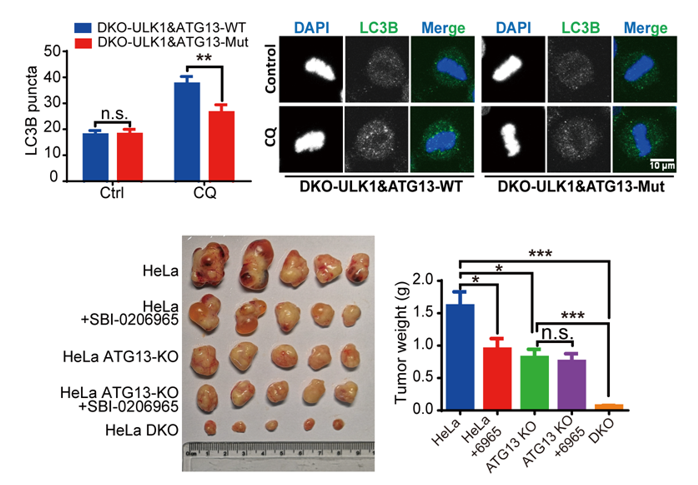
上圖顯示CDK1介導的ULK1/ATG13磷酸化促進(jìn)有絲分裂期自噬,下圖顯示ULK1/ATG13敲除在荷瘤小鼠模型中對腫瘤的抑制。
