電催化還原將硝酸鹽(NO3–)污染物轉化為高附加值的氨(NH3),為氮資源循環(huán)利用提供了一種有前景的解決途徑。NO3–轉化為NH3需要經(jīng)歷復雜的多步質(zhì)子電子轉移過(guò)程,導致動(dòng)力學(xué)速率緩慢、過(guò)電勢高。同時(shí),競爭性析氫反應(HER)降低了NH3法拉第效率及分電流密度。因此,硝酸鹽電催化還原(NO3–RR)的關(guān)鍵是設計制備高活性、高選擇性和高穩定性的催化劑。
由于Mn具有適當的軌道能量和對稱(chēng)的3d軌道,Mn-O位點(diǎn)有利于N2分子的吸附和活化,從而有助于實(shí)現高效電催化氮氣還原氨(NRR)。硝酸根N=O的鍵能(204 kJ mol-1)遠遠小于N≡N的鍵能(941 kJ mol-1),因此第一步的氫化反應往往是放熱過(guò)程,而氮還原的第一步氫化則是吸熱過(guò)程(且極有可能是決速步),所以在實(shí)驗上Mn-O位點(diǎn)更容易吸附和活化硝酸根。
基于此,固體所研究人員利用生物質(zhì)前驅體(細菌纖維素)表面富含的含氧官能團與金屬離子的配位作用,提出了一種在溫和條件下制備生物質(zhì)碳基材料負載的氧配位構型單原子錳催化劑的簡(jiǎn)單有效的策略。結合X射線(xiàn)精細結構吸收光譜(XAFS)、X射線(xiàn)光電子能譜(XPS),確定了催化劑中錳原子的配位結構和電子價(jià)態(tài)(圖1)。結合原位紅外和原位拉曼光譜分析,系統地研究了Mn-O-C電催化劑NO3–RR的反應機制。研究結果表明,單原子錳位點(diǎn)在特殊的配位環(huán)境(以四配位O原子為錨定的Mn原子,即Mn-(O-C2)4構型)具有高活性和高選擇性電催化硝酸鹽還原合成氨,在-0.5 V(vs. RHE)施加電位下實(shí)現了89.0 3.8%的高法拉第效率,在-0.7 V(vs. RHE)下獲得了1476.9 62.6 g h-1 cm-2的最高氨產(chǎn)率(圖2)。在流動(dòng)相電解池中,在100 mA cm-2的電流密度下,Mn-O-C顯示出最高的氨產(chǎn)率為3706.7 552.0 g h-1 cm-2,是H型電解池中氨產(chǎn)率的兩倍。
進(jìn)一步的密度泛函理論(DFT)分析表明,NO3-RR 表現為一系列脫氧(*NO3 *NO2 *NO *N)和加氫(*N *NH *NH2 *NH3)反應。Mn-O-C的高催化性能歸因于Mn-(O-C2)4活性中心,通過(guò)激活N-O鍵,改變中間體的吸附能和決速步驟(PDS)的自由能,以及抑制HER副反應,從而提高了電催化NO3-RR的選擇性。該工作為未來(lái)設計高效去除NO3--N的單原子錳電極提供了重要參考。
上述研究得到了國家自然科學(xué)基金、安徽省自然科學(xué)基金、中國博士后科學(xué)基金面上項目和站中特別資助項目的資助。
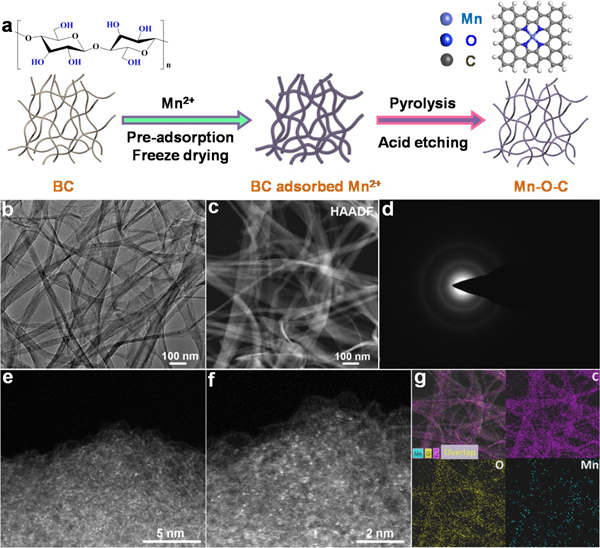
圖1. (a) Mn-O-C的合成路徑圖;Mn-O-C樣品的 (b) TEM圖, (c) HADDF-TEM圖, (d) SAED圖, (e)球差校正的HADDF-STEM圖和 (g) EDS元素分析圖。
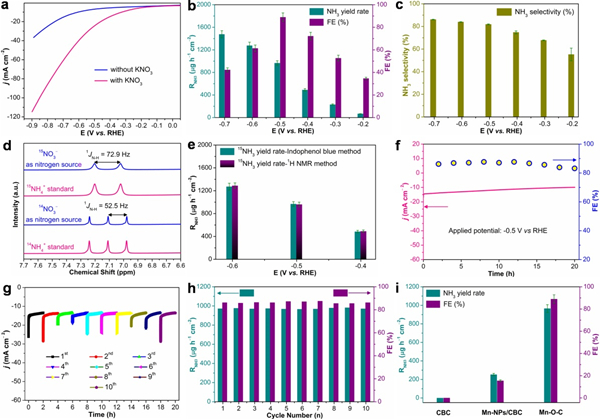
圖2. (a)Mn-O-C樣品分別在含有和不含有KNO3的Ar飽和的0.1 M K2SO4電解質(zhì)中對應的線(xiàn)性?huà)呙璺睬€(xiàn); (b)不同電位下對應的產(chǎn)氨速率和法拉第效率;(c)不同電位下的產(chǎn)氨選擇性; (d) 最佳電位下分別以15NO3和14NO3和標樣的1H NMR譜圖; (e) 最佳電位下靛酚藍和1H NMR兩種方法定量檢測氨速率對比圖;(f)長(cháng)時(shí)間NO3-RR測試;(g) 和 (h) 循環(huán)穩定性測試;(i) CBC,Mn-NPs/CBC 和Mn-O-C樣品NO3-RR性能對比圖。
